神田の異動に伴い、大気海洋研究所に移転しました。
リアルタイムPCR。
ミクロトーム。
インジェクションを行うための実体顕微鏡。このほかに、蛍光正立顕微鏡が2台。
カルシウムイメージングを行うEMCCDカメラ。
Oocyteクランプの実験セット。ゼノパス卵母細胞に強制発現させたチャネルの性質を解析する。
ポリプテルスセネガルス。繁殖まではOK。次は遺伝子導入。
ピラニアナッテリー。人工授精、遺伝子ノックアウトまで確立。
分子実験コーナー。
クリオスタット
分子実験コーナー(DNAゾーン)
パッチクランプ実験。GFP蛍光で光るニューロンの生きたままの発火活動を記録。
研究内容
メダカをはじめとする小型魚類の強みのひとつは、自分が知りたいと思う神経回路について、自分一人の手でトランスジェニック・ノックアウト個体の作出からパッチクランプ、カルシウムイメージングといった生理学的解析までの一連の研究を行えることです。脳自体が小さくスライスを作成する必要がないため、神経回路を遮断しない電気記録が可能です。もちろん、哺乳類を用いた研究の方が便利なことも多々あるので、哺乳類では困難なことを中心に研究を進めています。
現在、さまざまな神経回路について、主に形態学的、生理学的手法による神経回路の解明を、主にトランスジェニック/ノックアウトメダカを用いて行っています。非モデル動物を用いた研究
モデル動物だけでできることは限られています。そこで、モデル動物でできないこと、知りたいことは非モデル動物に、できるだけモデル動物のテクニックを応用して研究を進めます。現在は、ピラニアやポリプテルスなどを使っています。受精卵を得ることさえ出来れば、ゲノム編集や遺伝子組み換えなどの技術が利用可能になるので、研究の幅が大きく広がります。これら、モデル動物、非モデル動物を用いて、以下のような研究を行っています。このほかにも、まだ公表できないプロジェクトもあるので、詳細はお尋ねください。
- 脊椎動物HPG軸のプロトタイプを描く原理原則の解明
KO実験により、ほ乳類と魚類は、役者が同じでもまったく違う生殖制御をしていることがわかってきました(プレスリリース)。現在までにほ乳類では多くのメカニズムが理解されていますが、つまり、それはほ乳類に限ったことで、他の動物には応用できなことが多々あります。そのメカニズムを各種ノックアウトやトランスジェニックメダカなどをもちいて解明中です。 - 各種ペプチド神経系の機能解析・そのメカニズムの解析
なぜ生き物は陸上化できたのか。ホルモンの機能がかわった?ポリプテルスに遺伝子導入することで、陸上化させられるのでしょうか?チャレンジに向けた準備中です。 - 遺伝子が形を変えた原因ー進化の途上で起こったイベントを現生生物の形から調べる
クラウドファンディングでこのテーマについて実施しました。
一般向けの優しい言葉になっていますが、リンクをご覧ください。
形を変えるきっかけはなに?LH,FSHを別細胞化させた原因をさぐる
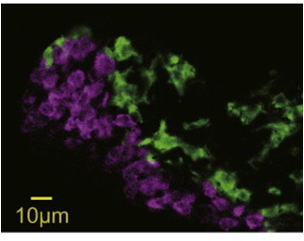 ※緑:FSH細胞、マゼンタ:LH細胞
※緑:FSH細胞、マゼンタ:LH細胞LH,FSHの遺伝子(lhb,fshb)は、真骨魚類では別々の細胞で発現している。
これは、同一の細胞で共発現している四足動物とは異なり、どうしてこのような違いが生まれたのか、を現在研究中である。
○環境変化に対応した中枢制御の変化
繁殖状態以外にも、個体の状態を変化させたときの脳内の遺伝子発現の変化を、定量的PCRや、in situ hybridization法での発現変動の解析を行い、研究を開始しています。
パラログ遺伝子の進化-余計に見えるパラログの適応度への貢献
GnRH神経系、およびキスペプチン神経系をはじめとする、神経内分泌に関与するニューロンの研究を行っています。
それらの神経系は、ゲノム重複によってうまれた複数のパラログ遺伝子を発現する複数の群から成ります(GnRH-1~3, kiss1~2;?生殖腺刺激ホルモンLH,FSHもパラログ)。形態学的特徴や、発現変動を観察することにより、それらのうちいずれが生殖に関与しているかを検証してきました。しかし、一度このように機能分化した遺伝子が、片方が機能しないときに補うことによって、個体の生存をサポートしてきたのではないかと考えられます。
現在、in situ hybridizationや免疫組織化学法による形態学的な観察や、遺伝子組み換え動物の作出、Zinc Finger Nuclease, TALEN,CRISPRをはじめとするノックアウト技術をモデル動物や、非モデル動物に応用することにより、進化のメカニズムを推測したいと考えています。